동향
Home > DB > 동향
| 기존 항암제 뛰어넘는 갑상선암 치료신약 한국서도 허가 | |||
|---|---|---|---|
| 분류 | 신약개발, 방사성요오드 치료, 갑상선암 | 조회 | 10807 |
| 발행년도 | 등록일 | 2015-10-12 | |
| 출처 | 뉴스1코리아 (바로가기) | ||
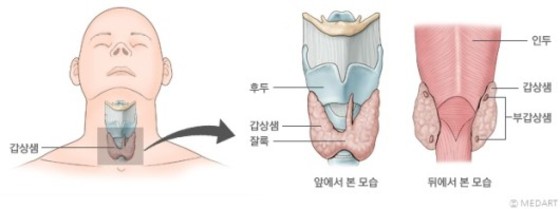 기존 방사성 요오드 치료로도 효과를 보이지 않는 갑상선암 환자들을 위한 치료 신약이 국내 허가를 받았다. 특히 지난해 1월 국내 최초, 식품의약품안전처로부터 같은 치료 적응증을 추가 획득한 표적항암제 넥사바보다 생존기간을 더 늘려 기대가 크다.
갑상선암은 보통 수술로 치료한다. 종양크기나 전이 범위 등을 고려해 수술을 진행한 뒤에도 재발 위험이 있는 경우 호르몬제를 복용하지만 재발 위험 고위험군 환자는 방사선 요오드 치료를 시행한다. 방사선 요오드 치료로도 효과를 보지 못하는 환자들의 경우 치료법이 매우 제한돼 이번 신약 허가는 이러한 환자들에 좋은 치료 옵션이 될 수 있다. 갑상선암은 아직 발병 원인이 정확하게 밝혀지지 않았으나 유전적인 요인이나 방사선 과량 노출 등이 위험요소로 지목되고 있다. 8일 제약업계에 따르면 일본계 제약사 에자이가 개발한 항암제 ‘렌비마캡슐’(성분 렌바티닙메실산염)이 지난 7일 식품의약품안전처 허가를 받았다. 올 초 일본과 미국에서 승인을 받은 데 이어 6월 유럽 허가 이후 약 4개월만인 한국에서도 신약 처방이 가능해졌다. 이 치료제는 '방사성 요오드치료에 효과가 없는 국소 재발성 또는 전이 진행성 분화 갑상선암’에 사용하는 효능으로 승인을 받았다. 성인에서 약 권장 투여용량은 1일 1회 24mg이고 매일 같은 시간에 식사와 관계없이 경구로 복용한다. 임상결과에 따르면 렌바티닙은 ‘방사성요오드치료 저항성 분화형 갑상선암(Pprogressive Radioiodine-refractory Differentiated Thyroid Cancer, RR-DTC)’ 환자의 생존기간을 위약군 대비 14.7개월 연장시켰다. 암환자에 있어서는 수개월의 생존기간 연장도 의미가 크다. 이는 100여개 임상기관에서 13개월 이내, 방사선 촬영 과정 중 병 진행이 확인된 RR-DTC 환자 392명에 대해 렌비마 1일 1회 24mg 투여용법으로 시행한 연구결과다. 위약투여군은 생존기간이 3.6개월인 반면 렌비마 투여군의 생존기간은 18.3개월이었다. 앞서 허가받은 넥사바의 경우 임상3상 연구에서 치료군 생존기간이 10.8개월로 위약군 생존기간 5.8개월보다 약 5개월 연장시켰다. 렌비마와 넥사바를 직접 비교한 임상데이터는 없으나 간접적으로 비교하면 렌비마를 통해 늘어난 생존기간이 훨씬 길다. 이에 미국 암치료 가이드라인(NCCN)도 렌비마 처방을 더 선호한다고 명시했다. 같은 목적의 치료제로는 이 두 약제뿐이다. 암이 없어지는 것을 뜻하는 ‘완전 관해’를 보인 환자비율도 렌바티닙 투여군에서 4명(1.5%)이 나왔고 위약 투여군에선 관찰되지 않았다. 다만 암이 없어졌더라도 완치는 보통 5년 생존율일 때를 말하는 경우가 많은데 이번 임상연구는 5년 이내로 진행된 것이어서 5년 생존율 환자 데이터는 없다. 부분 관해 비율은 렌바티닙 투여군 165명(63.2%), 위약군 2명(1.5%)이었다. 방사성요오드치료 저항성 분화 갑상선암(RR-DTC)은 수술과 방사성요오드치료법으로는 쉽게 치료할 수 없기 때문에 렌바티닙의 긴 생존기간 연장은 암환자 치료에 큰 의미가 될 전망이다. 렌비마는 갑상선암의 종양발생과 분화에 중요한 역할을 하는 것으로 알려진 혈관내피세포 성장인자(VEGFR)와 섬유모세포 성장인자 수용체(FGFR), 종양 유전자(RET) 활성을 동시에 억제하는 작용기전을 갖는 것으로 알려졌다. (후략)
|
|||
| 첨부파일 | |
다운로드수 | 0 |
|
|
 이전글 이전글 |
국가 R&D, 부처 협력·기업 수요 적극 반영한다 민·군 협력사업 등 부처 공동기획·개발…산업 연계 강화 |
|---|---|
 다음글 다음글 |
MIT Technology Review 선정 세상을 바꿀 10개의 혁신기술 |




